সালফার ট্রাইঅক্সাইড
সালফার ট্রাইঅক্সাইড একটি রাসায়নিক পদার্থ যার ফর্মুলা হলো SO3। গ্যাসীয় অবস্থায়, এই রাসায়নিক পদার্থটি একটি উল্লেখযোগ্য দূষণকারী, যা এসিড বৃষ্টির মূল এজেন্ট।[১] বাণিজ্যিক ভিত্তিতে প্রস্তুতের ক্ষেত্রে এটি সালফিউরিক অ্যাসিড তৈরির পূর্বের অবস্থা হিসাবে পাওয়া যায়।
| |||
| নামসমূহ | |||
|---|---|---|---|
| পছন্দসই ইউপ্যাক নাম
সালফার ট্রাইঅক্সাইড | |||
| পদ্ধতিগত ইউপ্যাক নাম
Sulfonylideneoxidane | |||
| অন্যান্য নাম
সালফিউরিক এনহাইড্রিড, সালফার (VI) অক্সাইড
| |||
| শনাক্তকারী | |||
ত্রিমাত্রিক মডেল (জেমল)
|
|||
| সিএইচইবিআই | |||
| কেমস্পাইডার | |||
| ইসিএইচএ ইনফোকার্ড | ১০০.০২৮.৩৬১ | ||
| ইসি-নম্বর |
| ||
| মেলিন রেফারেন্স | 1448 | ||
পাবকেম CID
|
|||
| আরটিইসিএস নম্বর |
| ||
| ইউএনআইআই | |||
| ইউএন নম্বর | UN 1829 | ||
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|||
| |||
| |||
| বৈশিষ্ট্য | |||
| SO3 | |||
| আণবিক ভর | 80.066 g/mol | ||
| ঘনত্ব | 1.92 g/cm3, liquid | ||
| গলনাঙ্ক | ১৬.৯ °সে (৬২.৪ °ফা; ২৯০.০ K) | ||
| স্ফুটনাঙ্ক | ৪৫ °সে (১১৩ °ফা; ৩১৮ K) | ||
| Reacts to give sulfuric acid | |||
| তাপ রসায়নবিদ্যা | |||
| স্ট্যন্ডার্ড মোলার এন্ট্রোফি এস |
256.77 J K−1 mol−1 | ||
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
−395.7 kJ/mol | ||
| ঝুঁকি প্রবণতা | |||
| নিরাপত্তা তথ্য শীট | ICSC 1202 | ||
ইইউ শ্রেণীবিভাগ (ডিএসডি)
|
|||
| আর-বাক্যাংশ | আর১৪, আর৩৫, আর৩৭ | ||
| এস-বাক্যাংশ | (এস১/২), এস২৬, এস৩০, এস৪৫, এস৫৩ | ||
| এনএফপিএ ৭০৪ | |||
| ফ্ল্যাশ পয়েন্ট | Non-flammable | ||
| প্রাণঘাতী ডোজ বা একাগ্রতা (LD, LC): | |||
LC৫০ (মধ্যমা একাগ্রতা)
|
rat, 4hr 375 mg/m3[তথ্যসূত্র প্রয়োজন] | ||
| সম্পর্কিত যৌগ | |||
অন্যান্য ক্যাটায়নসমূহ
|
Selenium trioxide Tellurium trioxide | ||
| Sulfur monoxide Sulfur dioxide | |||
সম্পর্কিত যৌগ
|
Sulfuric acid | ||
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |||
| তথ্যছক তথ্যসূত্র | |||

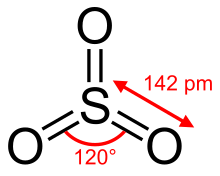
আণবিক কাঠামো এবং বন্ধন
সম্পাদনাভিএসইপিআর তত্ত্বের ভাষ্য অনুসারে, বায়বীয় সালফার ট্রাইঅক্সাইডের (SO3) হল ডিথ্রিএইচ (D3h) এর প্রতিসাম্য ত্রিভুজাকার প্ল্যানার অনু। সালফার ট্রাইঅক্সাইড ডিথ্রিএইচ পয়েন্ট গোষ্ঠীর অন্তর্ভুক্ত।
ইলেকট্রন-গণনার প্রথাগত পদ্ধতি অনুসারে, সালফারের পরমাণুতে অক্সিডেশন পর্যায়ে রয়েছে +৬ এবং এর ফরমাল চার্জ রয়েছে +২। লুইস কাঠামোটিতে রয়েছে সালফার (S) = অক্সিজেনের (O) ডাবল বন্ড এবং দুটি ডেটিভ বন্ড রয়েছে সালফার (S) - অক্সিজেনের (O) ডি-অরবিটাল ব্যবহার না করে।[২]
গ্যাসীয় সালফার ট্রাইঅক্সাইডের কোন বৈদ্যুতিক ডাইপোলার মোমেন্ট নেই। এটি সালফার (S) - অক্সিজেনের (O) বন্ডের মধ্যে থাকা ১২০ ডিগ্রি কোণের কারণে তৈরি হয়েছে।
কঠিন SO3 এর গাঠনিক কাঠামো
সম্পাদনাকঠিন আকারে থাকা সালফার ট্রাইঅক্সাইড (SO3) এর কাঠামোগত প্রকৃতিটি একটি চমকপ্রদ জটিল বিষয় কারণ এ সময় এর কাঠামোগত পরিবর্তন ঘটে পানির উপস্থিতি থাকায়।[৩] গ্যাসের ঘনীভূত করণের ফলে, একেবারে নির্ভেজাল SO3 একটি ট্রিমারে রূপে সংকুচিত হয়, যা প্রায়ই γ-SO3 নামে পরিচিত। এই আণবিক গঠনটি একটি বর্ণহীন কঠিন পদার্থ যার মেল্টিং পয়েন্ট ১৬.৪ °সে । এটি একটি চক্রাকার কাঠামো গ্রহণ করে যা [S(=O)2(μ-O)]3 হিসাবে পরিচিত।[৪]
যদি SO3 কে ২৭ °সে উপরে ঘনীভূত করা হয়, তাহলে α-SO3 গঠিত হয়, যার মেল্টিং পয়েন্ট হল ৬২.৩ °সে। α-SO3 দেখতে ফাইবারের মত হয়ে থাকে। কাঠামোগত ভাবে, এটি হল একটি পলিমার [S(=O)2(μ-O)]n। এই পলিমারের প্রতিটি প্রান্ত একটি হাইড্রক্সিল (OH) গোষ্ঠীর সাথে যুক্ত থাকে। β-SO3, আলফা ফর্মের মতই, এটি দেখতে ফাইবারের মত কিন্তু এর আণবিক ওজন ভিন্ন হয়ে থাকে, এতে একটি হাইড্রক্সিল-যুক্ত পলিমার থাকে, কিন্তু এর মেল্টিং পয়েন্ট হয় ৩২.৫ °সে। উভয় গামা ও বিটা ফর্ম মেটাস্ট্যাবল হয়ে থাকে, অর্থাৎ পর্যাপ্ত সময় দেয়া হলে এগুলো স্থিতিশীল আলফা ফর্মে রূপান্তরিত হবে। এই রূপান্তরটি ঘটে পানির উপস্থিতি থাকার কারণে।[৫]
একই সমান তাপমাত্রায় কঠিন SO3 এর আপেক্ষিক বাষ্পের চাপের মানের পার্থক্য হল আলফা < বিটা < গামা, এই মান এগুলোর আপেক্ষিক আণবিক ওজনকে চিহ্নিত করে। তরল সালফার ট্রাই অক্সাইডের বাষ্পের চাপ সুস্থিত থাকে এর গামা ফর্মের সাথে। সুতরাং একটি α-SO3 এর ক্রিস্টালকে তার গলনাঙ্কের তাপমাত্রায় উত্তপ্ত করা হলে হঠাৎ বাষ্পের চাপ বৃদ্ধি পাবে, এটা এতটাই শক্তিশালী যে গ্লাসের পাত্রে এটিকে উত্তপ্ত করা হচ্ছে সেটি ভেঙ্গে ফেলতে পারবে। এই প্রভাবটিকে বলে হয় "আলফা বিস্ফোরণ"।[৫]
SO3 হল প্রখররূপে হাইড্রোস্কোপিক। হাইড্রেশনের হলে উৎপন্ন তাপ সালফার ট্রাই অক্সাইডের (SO3) ও কাঠ বা তুলোর মিশ্রণে আগুন ধরাতে যথেষ্ট। এই সকল ক্ষেত্রে, SO3 ডিহাইড্রেড করে ঐ সকল কার্বোহাইড্রেটকে।[৫]
রাসায়নিক বিক্রিয়া
সম্পাদনাSO3 হল H2SO4 এর এনহাইড্রেড। ফলে, নিম্ন লিখিত রাসায়নিক বিক্রিয়াটি ঘটে:
- SO3 (g) + H2O (l) → H2SO4 (aq) (ΔHf= − ২০০ kJ mol−1)[৬]
বিক্রিয়াটি ঘটে একই সাথে দ্রুততার সাথে ও এক্সোথার্মিক ভাবে, যা বানিজিক ভিত্তিতে বৃহৎ আকারে উৎপাদনের জন্য খুবই ভয়ঙ্কর। ৩৪০ °সে বা এর উপরে সালফিউরিক এসিড, সালফার ট্রাই অক্সাইড ও পানি একই সাথে তাৎপর্যপূর্ণ ভাবে ঘনিভূত আকারে সাম্যাবস্থায় থাকে।
সালফার ট্রাই অক্সাইড একই সাথে সালফার ডাই ক্লোরাইডের সাথে বিক্রিয়া করে একটি প্রয়োজনীয় রিয়েজেন্ট থিনাইল ক্লোরাইড উৎপন্ন করে।
- SO3 + SCl2 → SOCl2 + SO2
SO3 হল একটি শক্তিশালী লুইস এসিড যা সহজেই তৈরি করে ক্রিস্টালাইন কমপ্লেক্স প্রিডিন, ডাইঅক্সেন ও ট্রাইমিথাইলমাইনের সাথে। এই সকল যৌগ ব্যবহৃত হয় সালফোনেটিং এজেন্ট রূপে।[৭]
প্রস্তুতি
সম্পাদনাসালফার ট্রাই অক্সাইড পরীক্ষাগারে প্রস্তুত করা হয় সোডিয়াম বাই সালফেটের দুই ধাপের পাইরোলাইসিসের মাধ্যমে। সোডিয়াম পাইরোফস্ফেট উৎপন্ন হয় এই দুই ধাপের মধ্যবর্তী ধাপে।[৮]
- ৩১৫ °সে তাপমাত্রায় ডিহাইড্রেশন করা হলে উৎপন্ন হয়:
- 2 NaHSO4 → Na2S2O7 + H2O
- ৪৬০ °সে যা ভেঙ্গে উৎপন্ন করে:
- Na2S2O7 → Na2SO4 + SO3
কিন্তু অপরদিকে পটাশিয়াম সালফেট (KHSO4) একই ধরনের রাসায়নিক বিক্রিয়া করে না।[৮]
বাণিজ্যিক ভাবে SO3 তৈরি করা হয় সংযোগ প্রক্রিয়ায়। সালফার ডাই অক্সাইড (SO2), যা তৈরি করা হয় সালফার বা আয়রন প্যারাইট (লোহার সালফেট আকরিক) কে পুড়িয়ে। যা পরবর্তিতে বিশুদ্ধ করা হয় ইলেক্ট্রোস্ট্যাটিক অধঃক্ষেপ প্রক্রিয়ায়, এরপর এটিকে অক্সিডাইজড করা হয় বায়ুর অক্সিজেনের সংস্পর্শে নিয়ে এসে প্রায় ৪০০ থেকে ৬০০ °সে তাপমাত্রায় ক্যাটালিষ্টের উপস্থিতিতে। একটি সাধারণত ব্যবহৃত ক্যাটালিষ্ট হল ভেনাডিয়াম পেন্টাঅক্সাইড (V2O5) যার সাথে উত্তেজক হিসাবে উপস্থিত থাকে পটাশিয়াম অক্সাইড (K2O) একই সাথে সহযোগী হিসাবে ব্যবহৃত হয় ডায়াটোমাইট বা সিলিকা। ক্যাটালিষ্ট হিসাবে প্লাটিনামও বেশ ভাল কাজ করে কিন্তু এটি অনেক দামী এবং ইম্পিউরিটি দ্বারা সহজেই অব্যবহার্য (দ্রুত কার্যকর) হয়ে ওঠে।[৯]
এই পদ্ধতিতে উৎপন্ন অধিকাংশ সালফার টাই অক্সাইড ব্যবহৃত হয় সালফিউরিক এসিড উৎপাদনে, তবে এতে সরাসরি পানি (H2O) যুক্ত করে এটি উৎপাদন করা হয় না , সরাসরি পানি যুক্ত করলে বাষ্পের কুয়াশা তৈরি করে, তবে অলিয়াম উৎপন্ন করা হয় ঘনিভুত সালফিউরিক এসিডে এটিকে সংযুক্ত করে ও পানির ডাইলেশন করার মাধ্যমে।
ব্যবহার
সম্পাদনাসালফার ট্রাইঅক্সাইড সালফেনেশন বিক্রিয়ার ক্ষেত্রে একটি অপরিহার্য বিকারক। এই বিক্রিয়াগুলো ডিটারজেন্ট, ডাই এবং ফার্মাসিউটিক্যালসের ইন্ডাস্ট্রির জন্য গুরুত্ব বহন করে। সালফার ট্রাইঅক্সাইড উৎপাদন করা হয় সালফিউরিক এসিড থেকে বা এই এসিড উৎপাদনে ব্যবহৃত হয়।
সতর্কতা
সম্পাদনাসালফার ট্রাইঅক্সাইড শ্বাসনালি এবং অন্ত্র উভয়ে মারাত্মক জ্বালা সৃষ্টি করতে পারে কারণ এটি প্রকৃতিগত ভাবে অত্যন্ত ক্ষয়কারী এবং পানিশোষনকারী হয়ে থাকে। সালফার ট্রাইঅক্সাইড অত্যন্ত সতর্কতার সাথে পরিচালনা করা উচিত কারণ এটি পানির সাথে তীব্রতার সাথে বিক্রিয়া করে এবং অত্যন্ত ক্ষয়কারী সালফিউরিক এসিড উৎপাদন করে।
সূত্র
সম্পাদনাআরও দেখুন
সম্পাদনাতথ্যসূত্র
সম্পাদনা- ↑ Thomas Loerting; Klaus R. Liedl (২০০০)। "Toward elimination of descrepancies between theory and experiment: The rate constant of the atmospheric conversion of SO3 to H2SO4"। Proceedings of the National Academy of Sciences of the United States of America। 97 (16): 8874–8878। ডিওআই:10.1073/pnas.97.16.8874।
- ↑ Terence P. Cunningham , David L. Cooper , Joseph Gerratt , Peter B. Karadakov and Mario Raimondi (১৯৯৭)। "Chemical bonding in oxofluorides of hypercoordinatesulfur"। Journal of the Chemical Society, Faraday Transactions। 93 (13): 2247–2254। ডিওআই:10.1039/A700708F।
- ↑ Inorganic chemistry। Academic Press। ২০০১-০১-০১। আইএসবিএন 0123526515।
- ↑ Advanced Inorganic Chemistry by Cotton and Wilkinson, 2nd ed p543
- ↑ ক খ গ Merck Index of Chemicals and Drugs, 9th ed. monograph 8775
- ↑ "সংরক্ষণাগারভুক্ত অনুলিপি" (পিডিএফ)। ২৭ জানুয়ারি ২০১৮ তারিখে মূল (পিডিএফ) থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২৬ এপ্রিল ২০১৭।
- ↑ Advanced inorganic chemistry। Wiley। আইএসবিএন 0471199575।
- ↑ ক খ http://doc.utwente.nl/68103/1/Vries69thermal.pdf
- ↑ Müller, Hermann (২০০০-০১-০১)। Sulfuric Acid and Sulfur Trioxide (ইংরেজি ভাষায়)। Wiley-VCH Verlag GmbH & Co. KGaA। আইএসবিএন 9783527306732। ডিওআই:10.1002/14356007.a25_635।